Física – Termologia – Termometria.
Durante muito tempo, esse assunto era tido como algo dissociado dos outros campos da física, especialmente de questões como mecânica, ótica, eletricidade. A separação era tal que havia um sistema de unidades próprio para avaliar as grandezas da Termologia. Só depois do advento das máquinas térmicas à vapor, à combustão interna se estabeleceu uma relação direta e íntima entre os estudos da Termologia e demais campos da física.
Tinha-se a ideia de que as sensações térmicas de quente e frio eram causadas por uma espécie de fluido que os corpos tinham capacidade de absorver e depois perder que causasse essas sensações.
Afinal o que é Termologia?
Nossa primeira noção a respeito do assunto vem das sensações de quente e frio que sentimos quando ocorre uma variação térmica do clima. No entanto essas sensações apenas nos mostram que há algo mudando no ar ao nosso redor e nossa pele acusa essa mudança, por meio dessas sensações.
Lâmpada elétrica. Produz luz, mas também emite calor.



Depois de muito pesquisar entendeu-se que o causador dessas sensações é a presença, em maior ou menor quantidade, de uma forma de energia, em geral denominada simplesmente de calor. Quando ligamos um queimador de gás, acendemos uma pequena pilha de lenha, ou mesmo uma vela ou lamparina, percebemos que esse fogo nos aquece a pele quando chegamos próximos a ele. Hoje sabemos que o fogo na verdade está transformando ou queimando energia química e transformando-a em energia térmica. Há inúmeras formas de transformar outras formas de energia em energia térmica, assim como podemos transformar energia térmica em outras formas. Exemplos disso são os motores de automóveis, máquinas em geral, acionadores de geradores elétricos, máquinas à vapor e muitas outras.
Em todas as situações citadas, há a presença de energia na forma de calor. Mas o que é afinal essa forma de energia?
Experimentos sofisticados conseguem mostrar que todas as moléculas, em qualquer estado físico, possuem um movimento vibratório em frequências suficientemente altas para que não sejam perceptíveis pelo nosso olho, até mesmo por suas dimensões pequeníssimas. Esse movimento implica num nível de energia interna de qualquer corpo. Quando alguma coisa, seja uma fonte de calor, o atrito ou impactos mecânicos o nível de vibração se eleva, a amplitude do movimento cresce e isso provoca a elevação de temperatura. A nossa percepção externa da variação da energia das moléculas é a variação de temperatura.
Calor é uma forma de energia ligada ao nível de vibração das moléculas da matéria.
Classicamente define-se:
Calor é o fluxo de energia em trânsito entre dois corpos ou partes de um corpo que se encontrem a temperaturas diferentes. As moléculas mais quentes (mais energia) influenciam as que estão próximas e dessa forma a energia se propaga de um lugar para o outro.
Termologia é o estudo das trocas de calor e seus respectivos efeitos.
Unidades de quantidade de calor
Sendo energia, a quantidade de calor também é medida com as unidades usadas em outras formas tais como energia mecânica (potencial e cinética). Assim:
- No SI (Sistema Internacional de Unidades) medimos a energia em joule (J).
- No MKgfS ou Sistema Técnico, medimos a energia em kgf.m ou kgm ( 1 kgm = 9,8\,J)
- No CGS a unidade de energia é erg e portanto a quantidade de calor também é erg.
- Quando os cientistas já haviam estabelecido um sistema de unidades para a Termologia, concluiu-se que era apenas uma forma diferente de energia. Por essa razão, algumas unidades continuam sendo usadas até os dias atuais e provavelmente continuarão em uso por muito tempo.
- A substância mais comum e de maior facilidade de manuseio em experimentos de calor é a água. Por isso a unidade básica para a quantidade de calor é definida tendo a massa de 1 grama de água como base.
- Caloria (1cal) é a quantidade de calor necessária para elevar de $l^0C$ a temperatura de $1,0\,g$ de água que se encontra inicialmente a $4^0C$.
- Existe um múltiplo que é a quilocaloria (1 kcal) tal que $1\,kcal = 10^3\, cal$
- O surgimento dos novos conhecimentos tornou necessário estabelecer a correlação entre as diversas unidades, para permitir a transformação entre elas. dessa forma chegou-se, por meio de experimentos, à conclusão de que: ${1,0 cal = 4,186\,J}$. Os tratados de nutrição costumam referir-se a uma unidade que aparentemente é incompatível com essa que vimos. No entanto eles apenas usam a chamada grande caloria que nada mais é do que um múltiplo, tal que ${1\,kcal = 10^3\,cal}$. Em algumas embalagens de alimentos já vem especificados os valores energéticos das porções na unidade quilocaloria ou grande caloria.
Termometria
É a parte da Termologia que estuda a variação da temperatura, usando para isso aspectos externos dos corpos, que variam com as mudanças do nível de vibração das moléculas. Por que usamos aspectos externos? É inviável fazer a medição do nível de energia das moléculas de modo direto, nas situações cotidianas.
-Os aspectos usados na avaliação das temperaturas, são as chamados Grandezas termométricas. Existem muitas grandezas que podem ser utilizadas, mas algumas são mais usadas por conta de sua praticidade. A primeira noção de temperatura que temos é a sensação de quente e frio. Essa sensação não é confiável pois pode variar de uma pessoa para outra, bem como é influenciada pelas condições precedentes. Se colocarmos uma das nossas mãos em água gelada e depois a colocarmos em água morna, teremos uma sensação térmica de que a nova temperatura está mais elevada do que realmente está. Se estamos caminhando na rua, num dia de sol forte, transpirando e chegamos à porta de um estabelecimento onde o ar é climatizado, temos uma primeira sensação de que o ambiente está gelado. Por isso recorremos à características mensuráveis como o comprimento, volume, pressão, cor, estado físico da matéria, nível de irradiação térmica, mudanças de estado para estabelecer escalas que permitam atribuir um valor aos diferentes estados térmicos de um corpo. Estas são então denominadas Grandezas termométricas.
Escalas termométricas
Para construir uma escala termométrica precisamos primeiramente escolher o que é denominado de pontos fixos. Estes são temperaturas onde determinados fenômenos sempre acontecem nas mesmas condições de pressão. Novamente entra em cena a água. Além de ser a substância mais abundante e comum disponível, ela apresenta dois pontos fixos bastante fáceis de obter. Estes são o ponto de fusão do gelo e o ponto de ebulição da água, nas condições normais de pressão atmosférica. Atribuindo valores a estes estados térmicos, podemos dividir o intervalo em partes iguais, obtendo assim uma escala termométrica de fácil reprodução.
Durante o desenvolvimento dos vários estágios de conhecimentos sobre a Termologia, foram estabelecidas várias escalas termométricas, entre as quais merecem ser vistas, mesmo estando algumas fora de uso.
Escala Fahrenheit
Diz uma lenda que, para criar sua escala, o matemático, físico e soprador de vidro, Daniel Gabriel Fahrenheit, de origem eslavo-germânica, teria atribuído o valor ${0^0F}$ ao estado térmico de um dia especialmente frio em Londres e ${100^0F}$ ao estado levemente febril de sua esposa, dividindo o intervalo em partes iguais. Mesmo que seja apenas lenda, existe um fundo de verdade nisso. Veremos depois que ${0^0F = -17,78^0C}$, ou seja bastante frio. Já ${100^0F = 37,75^0C}$, o que condiz com um estado febril leve.
Escala Celsius (Andrés Celsius)
Andrés Celsius recorreu à água para criar sua escala. Obteve gelo em fusão e atribuiu o valor ${0^0C}$ a esse estado térmico e depois colocou água em ebulição e atribuir a esse estado o valor ${100^0C}$.
Escala Reaumur
Criada por um pesquisador francês, talvez movido por questões de nacionalidade, usou também os mesmos pontos fixos usados por Celsius, porém atribuiu o valor $80^0Re$ ao ponto de ebulição da água.
O aprofundamento das pesquisas, levou à busca por uma escala absoluta, isto é, que atribuísse o valor $0^0$ à menor temperatura possível na natureza. Coube ao engenheiro e pesquisador Lord Kelvin a determinação desse ponto. Conseguiu-se, por meios indiretos, obter o valor de $ -273,15^0C$. É impossível levar uma porção de matéria ao zero absoluto, por métodos termodinâmicos, mas foi possível chegar bem perto. Nestas condições a matéria passou a apresentar fenômenos como supercondutividade e superfluidez. Tendo sido baseada na Escala Celsius, temos que a variação de ${1^0C = 1\,K}$. Já na escala Fahrenheit, o valor do zero absoluto é de ${-459,67^0F}$. Há uma outra escala absoluta (em desuso) denominada Rankine e nela o zero absoluto também é ${0 R}$ e sua graduação está baseada na Fahrenheit.
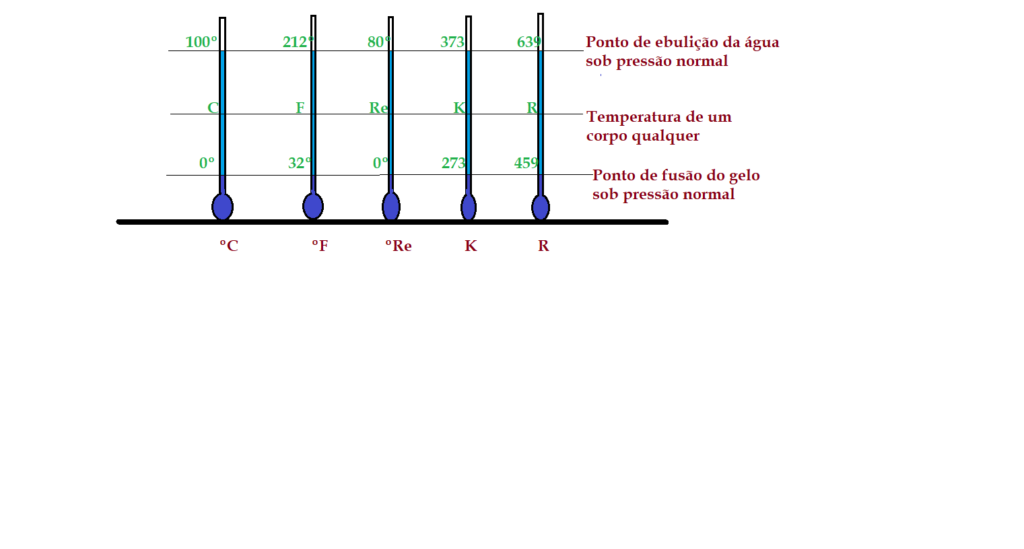
Analisando a figura e estabelecendo uma proporcionalidade entre os intervalos nas diferentes escalas teremos:
${{{C – 0}\over{100 – 0}} = {{F – 32}\over{212 – 32}} = {{Re – 0}\over{80 – 0}} = {{K – 273}\over{373 – 273}} = {{R – 459}\over{639 – 459}}}$
Efetuando as operações e simplificando os denominadores teremos:
${{{C}\over{5}} = {{F – 32}\over{9}} = {{Re}\over{4}}= {{K – 273}\over{5}} = {{R – 459}\over{9}}}$
Temos pois três escalas relativas e duas absolutas, sendo que uma relativa e uma absoluta caíram em desuso, provavelmente por serem menos práticas. A escala mais usada mundialmente é a Celsius, sendo que nos países de colonização inglesa ainda se usa frequentemente a Fahrenheit.
Hora de exercitar
- Em um dia especialmente quente no deserto, um termômetro Fahrenheit indica a temperatura de ${122^0F}$. Se fosse usado um outro graduado na escala Celsius, qual seria o valor indicado?
Temos que: ${{{c}\over{5}} = {{F – 32}\over{9}}}$
Se F = 122^0F, então: ${{{C}\over{5}} = {{122 – 32}\over{9}}}$
${{C} = {{5}\cdot{90}}\over{9}}$$\Rightarrow$${ C = 50ºC}$
2. Uma enfermeira usa inadvertidamente um termômetro graduado na escala Fahrenheit, quando estava acostumada a usar um Celsius. A fazer a leitura, sofreu um choque pois o mesmo indicava ${96,8^0}$. Chamou o médico e lhe mostrou o termômetro. Vendo tratar-se de um aparelho diferente, o médico a tranquilizou, dizendo que a temperatura estava normal. Qual era a temperatura do paciente?
${\theta = 96,8^0F}$
${{{C}\over{5}} = {{F – 32}\over{9}}}$
${{{C}\over{5}} = {{96,8 – 32}\over{9}}}$
${{C} = {5}\cdot{{64,8}\over{9}}}$
${C = {5}\cdot{7,2}}$$\Rightarrow$ ${C = 36ºC}
3. Se uma porção de álcool entra em ebulição na temperatura de 85^0C, determine o valor dessa temperatura nas escalas Fahrenheit e Kelvin.
${{{C}\over{5}} = {{F – 32}\over{9}} = {{K – 273}\over{5}}}$
Se temos ${\theta = 85^0C}$, vamos substituir e calcular.
${{{85}\over{5}} = {{F – 32}\over{9}}}$
${{17}\cdot{9} = {F – 32}}$$\Rightarrow ${4 = {153 + 32}}$
${F = 185ºF}$
${{{85}\over{5}} = {{K – 273}\over{5}}}$
Cancelando os denominadores que são iguais
${{85} = {K – 273}}$$\Leftrightarrow$ ${K = {85 + 273} = 358K}$
Logo: ${\theta = 85^0C = 185^0F = 358K}$
4. Uma porção de água sofre uma elevação de sua temperatura em 12^0C; se for usado um termômetro Fahrenheit, qual seria o valor dessa elevação de temperatura, nas mesmas condições?
Vejamos qual é o valor da elevação de $1^0C$, na escala Fahrenheit. Podemos fazer isso substituindo nas razões de conversão, os numeradores por uma variação Assim $\Delta ^0C$; $\Delta^0F$ ou $\Delta^0R_{e}$
${\Delta^0C\over 5} = {\Delta^0F\over 9} = {\Delta^0R_{e}} = {\Delta K\over 5}={\Delta R_{e}\over4}$
Se $\Delta^0C = 12ºC$ fica:
${12\over5} = {\Delta^0F\over 9}$
${{12\cdot 9}\over 5} = \Delta^0F$$\Leftrightarrow$$\Delta^0F = 21,6^0F$
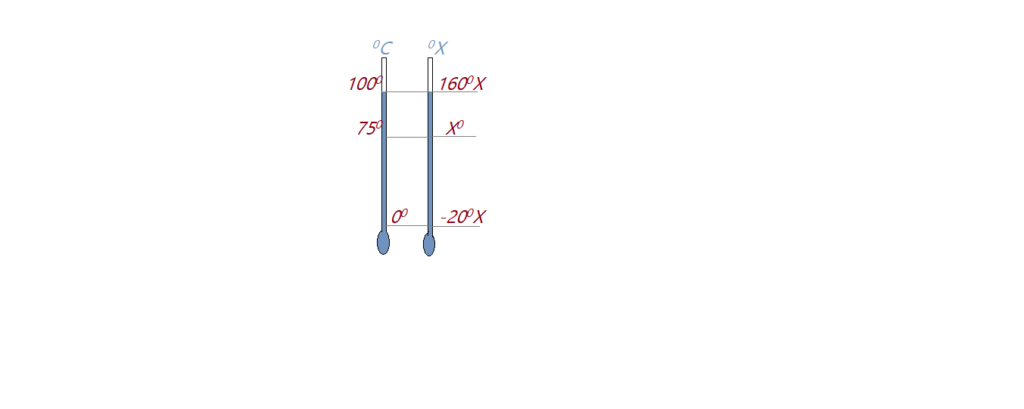
05. Uma escala termométrica $X$, atribui o valor $-20^X$ ao ponto do gelo e $140^0X$. Estabeleça a proporção que essa escala tem em relação à escala Celsius e depois determine o valor correspondente nessa nova escala à temperatura $\theta = 75^0C$.
Observando a figura acima, vemos que existe entre as duas escalas a mesma forma de relação que usamos entre as demais escalas. Podemos então escrever:
$$\frac{C- 0}{100-0} = \frac{X – (-20)}{160-(-20)}$$
$\frac{C}{100} = \frac{X + 20}{160 + 20}$$\Leftrightarrow$$\frac{c}{100} = \frac{X + 20}{180}$
Simplificamos os denominadores, multiplicamos por $20$.
$\frac{C}{100}\times 20 = \frac{X + 20}{180}\times 20$
$$\color{Navy}{\frac{C}{5} = \frac{X + 20}{9}}$$
O valor correspondente à $75^0C$, obtemos por essa proporção.
$\frac{75}{5} = \frac{X + 20}{9}$$\Leftrightarrow$$ X + 20 = 9\times {15}$
$X = 135 – 20 = 115^0X$
$$\color{Navy}{75^0 = 115^0X}$$
Vamos exercitar sozinhos agora
- Um termômetro indica 70^0C. Qual seria o valor indicado por um outro graduado em escala Fahrenheit nas mesmas condições? E um Kelvin?
- Se a temperatura absoluta de um líquido é ${\theta = 345K}$. Quanto indicaria um termômetro Celsius nas mesmas condições? E um Fahrenheit?
- Em que condições dois termômetros, um Celsius e um Fahrenheit indicarão a mesma leitura?
- Uma escala termométrica foi construída tomando por ponto fixo ${-20^0X}$ para o ponto do gelo e ${140^0X}$ para o ponto do vapor. Estabeleça a equação de conversão entre essa escala e a escala Celsius e também da escala Fahrenheit.
- Se um termômetro for graduado na escala Reaumur e estiver indicando a temperatura ${\theta = 35^0Re}$, qual seria a leitura equivalente num termômetro Fahrenheit? E num Celsius?
- Qual seria a leitura absoluta da temperatura do exercício anterior tanto na escala Kelvin, quanto na Rankine?
- Calcule qual é a elevação de temperatura na escala Celsius que equivale à uma elevação de $108^0F$. Verifique qual seria a mesma variação, usando-se uma escala Reumur.
- Um termômetro é graduado usando-se para ponto de fusão do gelo o valor $-25^0Y$ e para o ponto do vapor (ebulição da água) o valor $175^0Y}. Estabeleça a relação de conversão entre esse termômetro, um Celsius e um Fahrenheit.
Havendo dúvidas, pergunte para que eu possa esclarecer. Mesmo se for um exercício de outra origem, não há problema. Tentarei ajudar do mesmo modo.
Curitiba, 28 de setembro de 2019
Décio Adams
www.facebook.com/livros.decioadams
www.facebook.com/decioadams.matfisonline
Telefone: (41) 3019-4760
Celular e WhatsApp: (41) 99805-0732
