FI.ME-015.01. Física – Mecânica, estática. Massa específica, densidade e peso específico.
Massa específica.
Por incrível que pareça, já Arquimedes, há mais de 200 anos antes de Cristo, percebeu que os diferentes materiais, apresentam massas diferentes, em volumes iguais. Tanto isso é verdade que o conhecido Princípio de Arquimedes, sobre empuxo, tem a densidade como base. Densidade e massa específica não são sinônimos, porém são intimamente ligadas. Muitos autores denominam a massa específica de densidade absoluta. Foi essa a forma encontrada pelo cientista grego para provar que a coroa do rei não era de ouro maciço e sim feita de outro metal, recoberto de ouro. Vamos falar nos detalhes depois.
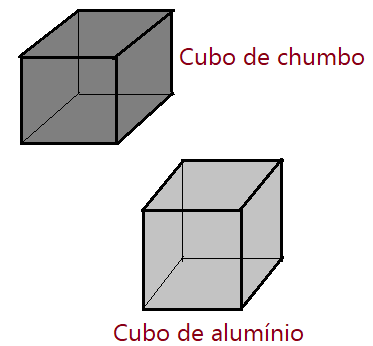
Se colocarmos dois cubos de mesmo volume, sendo um feito de chumbo e o outro de alumínio, sobre uma balança, verificaremos uma significativa diferença em sua massa. Assim fica evidente que existe diferença entre a natureza dos dois metais.
- “A massa específica de uma substância é obtida pela divisão da massa de um corpo dela constituído, pelo seu respectivo volume”.
Usamos para representar a grandeza, a letra grega “mi”, a massa por $m $ e o volume por $V$. Teremos então:
- $\bbox[5px,border:2px solid Olive]{\color{Navy}{\mu = {m\over V}}}$
Sendo as unidades de massa no SI o $\color{Navy}{m = quilograma (kg)}$ e volume o metro cúbico $\color{Navy}{V = m^3}$, teremos como unidade de massa específica o:
- $\bbox[4px,border:2px solid Olive]{\color{Navy}{\mu = kg/m^3}}$
A unidade de massa específica é pois o quociente da unidade de massa, pela unidade de volume no sistema de unidades que se está usando.
Vamos citar algumas outras unidades que poderão aparecer, se o sistema de unidades usado não for o SI. Veja os exemplos:
- $\color{Navy}{g/cm^3}$; $\color{Navy}{utm/m^3}$; $\color{Navy}{g/l}$; $\color{Navy}{ton/m^3}$
É possível estabelecer relações entre as unidades nos diferentes sistemas de unidades. Para isso precisamos da relação entre as unidades de massa e de volume. Vejamos:
- $\color{Navy}{1 kg = 10^3 g}$
- $\color{Navy}{1m^3 = 10^6 cm^3}$
Substituindo as unidades na razão da massa específica, teremos:
- $\color{Navy}{1\,kg/m^3= \frac{10^3 g}{10^6\,cm^3}}$
- $\color{Navy}{1\,kg/m^3 = 10^{-3}\,g/cm^3}$
Se fizermos a transformação inversa, iremos ter:
- $\color{Navy}{1\,g/cm^3 = 10^3\,kg/m^3}$
Procedendo de modo análogo iremos ter:
- $\color{Navy}{1\,kg/m^3= 1,0\,g/l}$
- $\color{Navy}{1\,utm/m^3= 9,8\,kg/m^3}$
- $\color{Navy}{1\,kg/m^3 = \frac{1}{9,8}utm/m^3}$
Algum exercício vai bem!
01. Determine a massa de um paralelepípedo de chumbo, medindo $\color{Sepia}{c = 20\,cm}$, $\color{Sepia}{l = 12\,cm}$ e $\color{Sepia}{h = 10\,cm}$, sabendo que a massa específica do chumbo $\color{Sepia}{\mu_{Pb}= 11, 34\,g/cm^{3}}$.
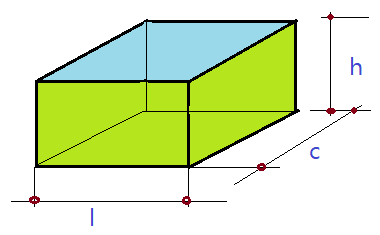
Calcularemos primeiro o volume do sólido.
$$\color{Maroon}{V = c\times l\times h}$$
$V = 20,0\times 12\times 10 = 2400,0\,cm^{3}$
$\mu_{Pb} = \frac{m}{V}$$\Leftrightarrow$$ m = \mu_{Pb}\times V$
$m = 11,34\times 2400,0 = 27216,0\,g$
O paralelepípedo tem massa igual a:
$$\color{Navy}{m = 27216,0\,g}$$
02. Determine a aresta de um cubo de ferro, cuja massa é $\color{Sepia}{m = 62,96\times 10^{3}\,kg}$. Sabendo que a massa específica do ferro é $\color{Sepia}{\mu_{Fe}=7,87\times 10^{3}}$.
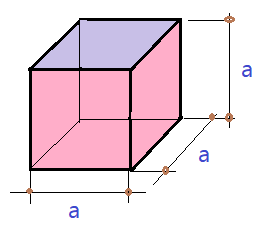
Começaremos pela determinação do volume, a partir da definição de massa específica.
$$\color{Maroon}{\mu = \frac{m}{V}}$$
$V= \frac{m}{\mu_{Fe}}$$\Leftrightarrow$$V = \frac{62,96\times 10^{3}}{7,87\times 10^{3}}$
$V = 8,0\,m^{3}$
O volume de um cubo é a aresta elevada ao cubo. Logo:
$$\color{Maroon}{V= a^{3}}$$
$\sqrt{3}{a^{3}} = \sqrt[3]{8}$$\Leftrightarrow$$a = 2,0\,m$
O cubo tem aresta de:
$$\color{Navy}{a = 2,0\,m}$$
03. Uma viga de concreto mede $\color{Sepia}{3,0\,m}$ de comprimento, tem $\color{Sepia}{0,50\,m}$ de altura e $\color{Sepia}{0,25\,m}$ de largura. Se sua massa é de $\color{Sepia}{m=900\,kg}$, determine a massa específica do material que constitui a viga.
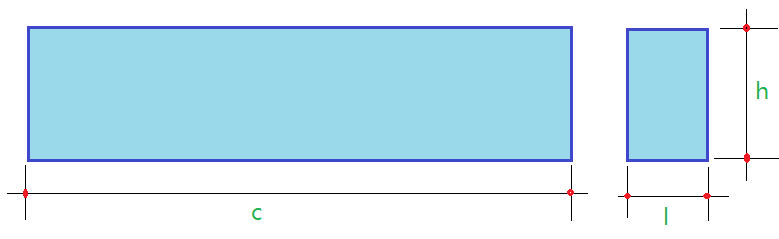
Vejamos o volume da viga, que tem a forma de um paralelepípedo.
$$\color{Maroon}{V = c\times l\times h}$$
$V = 3,0\times 0,50\times 0,25 = 0,375\, m^{3}$
Aplicando a definição de $\mu$, temos:
$$\color{Maroon}{\mu_{con}= \frac{m}{V}}$$
$\mu_{con} = \frac{900,0}{0,375} = 2400,0\,kg/m^{3}$
O concreto dessa viga tem massa específica de:
$$\color{Navy}{\mu_{con}= 2400,0\,kg/m^{3}}$$
04. Um tanque feito de alumínio, mede externamente $\color{Sepia}{c= 1,2\,m}$, $\color{Sepia}{l = 0,80\,m}$ e $\color{Sepia}{h=0,60\,m}$, tendo suas paredes de $\color{Sepia}{e = 6,0\,mm}$ de espessura. A massa específica do alumínio é $\color{Sepia}{\mu_{Al}= 2,7\,g/cm^{3}}$. O tanque contém água até a altura de $\color{Sepia}{h_{H_{2}O}= 35\,cm}$ e $\color{Sepia}{h_{ól}= 20\,cm}$. Sabemos que a água tem massa específica de $\color{Sépia}{\mu_{H_{2}O}=1,0 g/cm^{3}}$ e o óleo $\color{Sepia}{\mu_{ól}=0,78\,g/cm^{3}}$. Determine a massa específica média do tanque com os líquidos.
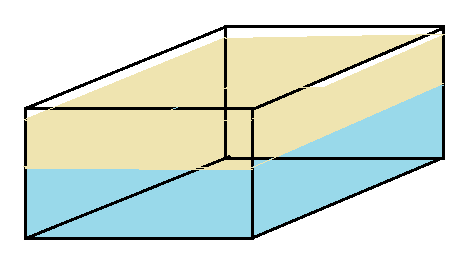
Temos três tipos de materiais. O Alumínio que contém os líquidos, a água e o óleo. É pois necessário determinar os volumes e massas de cada um, somar e por fim obter a massa específica média do conjunto. Vamos resolver tudo isso no SI.
Tanque. São seis faces, congruentes duas a duas. Todas as faces tem a mesma espessura.
Fundo e tampa ou face superior.
$V_{1}= 1,2\times 0,80\times 6,0\times 10^{-3} = 5,76\times 10^{-3}\,m^{3}$
Faces laterais (comprimento)
$V_{2}= 1,20\times 0,60\times 6,0\times 10^{-3}= 4,32\times 10^{-3}\,m^{3}$
Extremidades.
$V_{3}= 0,80\times 0,60\times 6,0\times 10^{-3} = 2,88\times 10^{-3}\,m^{3}$
O volume de alumínio do tanque é então:
$V = 2\times {(V_{1} + V_{2} +V_{3})} = 2\times{[(5,76 + 4,32 + 2,88)\times 10^{-3}]} = 0,02592\,m^{3}$
A massa de alumínio que forma o tanque será então:
$m = \mu_{Al}\times V$$\Leftrightarrow$$m=2,7\times 10^{3}\times 2,592\times 10^{-2}$
$m_{Al} = 69,984\,kg$$\Rightarrow$ massa de alumínio.
Volume de água:
$V_{H_{2}O}= 1,188\times 0,788\times 0,35 = 0,3276\,m^{3}$
$m_{H_{2}O} = 0,3276\times 10^{3} = 3,276\times 10^{2}\,kg$$\Rightarrow$ massa de água.
Volume do óleo.
$V_{ól}= 1,188\times 0,788\times 0,20 = 0,1872\,m^{3}$
$m_{ól} = 0,1872\times 780 = 143,04\,kg$$\Rightarrow$ massa do óleo.
Massa do conjunto.
$m = m_{Al} + m_{H_{2}O} + m_{ól}$$\Leftrightarrow$$m= 67,392 + 327,6 + 143,04 = 540,624\,kg$
Volume externo do tanque:
$V= 1,20\times 0,80\times 0,60 = 0,576\,m^{3}$
$\mu_{ap}= \frac{m}{V}$$\Leftrightarrow$$\mu_{ap}= \frac{540,624}{0,576}= 938,583\,kg/m^{3}$
A massa específica aparente ou média do conjunto é então de:
$$\color{Navy}{\mu_{ap}=938,583\,kg/m^{3}}$$
Em números redondos iríamos considerar.
$$\color{Navy}{\mu_{ap}=939,0\,kg/m^{3}}$$
Tabela de algumas massas específicas
| Substância | Unidade($kg/m^{3}$$ | Observações |
| Meio interestelar | $10^{-25} – 10^{-15}$ | $90\% H; 10\%He$ variável |
| Atmosfera terra | $1,2$ | Ao nível do mar |
| Ar(padrão) | $1,2$ | a 0ºC e 1 atm |
| Cortiça | $240 – 260$ | |
| Aerogel | $1 – 2 $ | |
| Água | $1000$ | nas CNTP |
| Água do mar | $1030$ | |
| Gelo | $940$ | |
| Plástico | $850 – 1400$ | Polipropileno, PET/PVC |
| Terra | $5520$ | Massa específica média. |
| Cobre | $8920 – 8960$ | Temperatura ambiente |
| Chumbo | $11340$ | |
| Tungstênio | $19250$ | |
| Ouro | $19330$ | 24 k (Puro) |
| Ouro puro fundido | $19250$ | |
| Núcleo da Terra | $\simeq 13000$ | |
| Urânio | $18950$ | |
| Irídio | $22650$ | |
| Ósmio | $22610$ | Na temperatura ambiente |
| Núcleo do Sol | $160000$ | |
| Núcleo atômico | $\simeq 3.10^{17}$ | |
| Estrela de Nêutrons | $8,4.10^{16}-1.10^{18}$ | |
| Gasolina | $680$ | |
| Álcool etílico | $789$ | |
| Mercúrio | $13400$ | |
| Glicerina | $1260$ | |
| Alumínio | $2700$ | |
| Platina | $21400$ | |
| Óleo SAE 30 | $912$ | |
| Prata | $10500$ | |
| Ferro | $7870$ | |
| Níquel | $8910$ | |
| Cromo | $7100$ |
Densidade.
Disse acima que densidade e massa específica são “parentes”. Há quem afirme que são sinônimos. A diferença entre as duas coisas é:
- Densidade$\rightarrow$ é um número, sem unidade. Tem valor idêntico em qualquer sistema de unidades utilizado.
- Massa específica$\rightarrow$ tem valor diferente em cada sistema de unidades. Seu valor é diferente em cada sistema de unidades.
- Obs.: Iremos denominar a massa específica de densidade absoluta, como boa parte dos autores faz.
A determinação da densidade de uma substância é feita dividindo-se a massa específica dessa substância, à determinada temperatura, pela massa específica da água, à $4^0C$. Isso por ser essa a temperatura em que a água tem o menor volume. A unidade padrão de massa $\color{Maroon}{1g}$ é definida como a massa de $\color{Maroon}{1\,cm^3}$ de água na temperatura de $\color{Maroon}{\theta\simeq 4^0C}$.
- $$\color{Navy}{\delta = \frac{\mu_{S}}{ \mu_{H_{2}0}}}$$
Alguns exemplos.
- A massa específica da água no SI é:
- $\color{Navy}{\mu_{H_{2}O} = 10^3 kg/m^3}$
- No CGS teremos:
- $\color{Navy}{\mu_{H_{2}O} = 1 g/cm^3}$
- No MKgfS, será:
- $\color{Navy}{\mu_{H_{2}O} = {9,8\times 10^3}utm/m^3}$
- $\color{Navy}{\mu_{H_{2}O} = 10^3\,g/l = 1,0\,kg/l}$
O mercúrio tem massa específica:
- $\color{Navy}{\mu_{Hg} =13,6\,g/cm^3 = 13,6\times 10^3\,kg/m^3}$
Vamos determinar a densidade do mercúrio em relação à água, tomada geralmente como referência.
- $\color{Navy}{\delta_{Hg} = {{\mu_{Hg}}\over{\mu_{H_{2}O}}}}$
- $\color{Navy}{\delta_{Hg} = {{13,6g/cm^3}\over {1g/cm^3}} = 13,6}$
- $\color{Navy}{\delta_{Hg} = {13,6\times 10^3{kg/m^3}}{10^3{kg/m^3}}= 13,6}$
Note que o valor da densidade não depende do sistema de unidades. Ela representa quantas vezes uma unidade de volume de mercúrio, contém a massa de igual volume de água à temperatura de $\color{Maroon}{\theta=4^0C}$$.
Densidade relativa entre substâncias
Assim como podemos determinar a densidade de uma substância qualquer em relação à água, podemos determinar a densidade de uma substância em relação a outra, nas mesmas condições de temperatura.
Sejam as substâncias A e B. A massa específica de A será $\color{Sepia}{\mu_{A}}$ e de B será $\color{Sepia}{\mu_{B}}$. Se quisermos determinar a densidade de A em relação a B, faremos:
$$\color{Brown}{\delta_{AB} = \frac{\mu_{A}}{\mu_{B}}}$$
De B em relação a A, basta inverter as posições na divisão.
$$\color{Sepia}{\delta_{BA} =\frac{\mu_{B}}{\mu_{A}}}$$
01. Vamos determinar a densidade do chumbo em relação à prata, depois da prata em relação ao chumbo. Sendo $\color{Sepia^{\mu_{Pb}=11,34\times 10^{3}\,kg/m^{3}}$ e $\color{Sepia}{\mu_{Ag} = 10,50\times 10^{3}\,kg/m^{3}}$.
$$\color{Maroon}{\delta _{PbAg} = \frac{\mu_{Pb}}{\mu_{AgPb}}}$$
$\delta_{PbAg} =\frac{11,34\times 10^{3}}{10,50\times 10^{3}} = 1,08$
$$\color{Navy}{\mu_{PbAg} = 1,08}$$
Isso nos indica que volumes iguais de chumbo e prata, a massa do chumbo é 1,08 vezes a massa de prata.
$$\color{Maroon}{\mu_{AgPb}=\frac{\mu_{Ag}}{\mu_{Pb}}}$$
$\mu_{AgPb}=\frac{10,50\times 10^{3}}{11,34\times 10^{3}} = 0,926$
$$\color{Navy}{\mu_{AgPb}= 0,926}$$
Então podemos afirmar que, em volumes iguais de prata e chumbo, a massa de prata é igual a $92,6\%$ da massa do chumbo.
02. Um cálice litúrgico, usado em celebrações religiosas, tem massa $\color{Sepia}{m = 768,9\,g}$. Sua composição é liga de ouro e prata, cujas massas específicas são respectivamente $\color{Sepia}{\mu_{Au}=19,33\,g/cm^{3}}$ e $\color{Sepia}{\mu_{Ag}=10,50\,g/cm^{3}}$. Quer-se saber o volume desses dois metais que foram misturados para obter a matéria prima usada na confecção do cálice. Para isso, encheu-se uma bacia totalmente de água e nela mergulhou suavemente o cálice, para transbordar somente o volume deslocado pelo objeto. A água que transbordou foi colhida e colocada em uma proveta, onde se obteve a indicação de $\color{Sepia}{V = 48\,cm^{3}}$. Determinemos agora quanto desse volume é ouro e quanto é prata.
A água derramada nos informa o volume de metal existente no cálice. De posse do volume e da massa, podemos calcular a densidade média do objeto.
$$\color{Maroon}{\mu = \frac{m}{V}}$$
$\mu_{cal}= \frac{768,9}{48}= 16,019\,g/cm^{3}$$|Rightarrow$ massa específica da liga de que foi feito o cálice.
Temos então o volume total e a massa específica da liga.
$V = V_{Au} + V_{Ag}$$\Leftrightarrow$$ 48 = V_{Au} + V_{Ag}$ (I)
$m = \mu_{Au}\times V_{Au} + \mu_{Ag}\times V_{Ag}$$\Leftrightarrow$$768,9 = 19,33\times V_{Au} + 10,50\times V_{Ag}$ (II)
Temos duas expressões para os volumes de ouro e prata. Isolando uma das variáveis na primeira e substituindo na segunda, chegaremos ao resultado.
$V_{Au} = 48 – V_{Ag}$
$768,9 = 19,33\times({48 – V_{Ag}}) + 10,5\times _{Ag}$$\Leftrightarrow$$768,9 = 927,84 – 19,33\times V_{Ag} + 10,5\times V_{Ag}$$768,9 – 927,84 = 10,5\times V_{Ag} – 19,33\times V_{Ag}$$\Leftrightarrow$$- 158,94 = – 8,83\times V_{Ag}$
$V_{Ag} = \frac{-158,94}{- 8,83}$$\Leftrightarrow$$V_{Ag} = 18\,cm^{3}$
$V_{Au} = 48 – V_{Ag}$$\Leftrightarrow$$V_{Au}= 48 – 18 = 30\,cm^{3}$
O cálice é confecionado com a liga de $18cm^{3}$ de prata e $30cm^{3}$ de ouro, o que corresponde a um percentual de $62,5\%$de outo e $37,5\%$ de prata.
Podemos demonstrar esses percentuais por regra de três.
$ 100\% = 48\,cm^{3}$
$ x = 30\,cm^{3}$$\Leftrightarrow$$ x = \frac{100 x 30}{48} = 62,5\%$
$ x = 18\,cm^{3}$$\Leftrightarrow$$ x = \frac{100\times 18}{48}= 37,5\%$
Peso específico
- O peso específico de uma substância representa o peso existente em uma unidade de volume da substância.
- $$\color{Navy}{\rho = frac{P}{V}}$$
Como o peso é obtido multiplicando a massa do corpo pela aceleração da gravidade, podemos também determinar o peso específico multiplicando a massa específica pela aceleração da gravidade.
- $\rho = \frac{m\times g}{V}= \frac{m}{V}\times g$
- $\color{Navy}{\rho = {\mu\times g}}$
Vamos calcular o peso específico do ouro. Temos que:
- $\color{Navy}{\mu_{A_u}= 19,3\times 10^3\,kg/m^3}$
- $\color{Navy}{\rho_{A_u} = \mu_{A_u}\times g = {19,3\times 10^3}\times {9,8}}$
- $\color{Navy}{\rho_{A_u} = {19,3\times 10^3}\times {9,8} = 188,16\times 10^3\,N/m^3 =18,82\times 10^4\,N/m^3}$
Vamos exercitar um pouco o que vimos hoje. Outro dia caminhamos mais um pouco.
- Um bloco de alumínio tem aresta de $\color{Sepia}{0,3\,m}$. A massa específica do alumínio é $\color{Sepia}{2,7.10^3\,kg/m^3}$. Qual é a massa desse bloco?
Se a aresta é $a = 0,3\,m$, trata-s de um cubo e o volume é essa aresta elevada à terceira potência.
$\color{Maroon}{V = a^{3}}$
$V = 0,3^{3} = 0,027\,m^{3}$
$$\color{Maroon}{\mu = \frac{m}{V}}$$
$m = \mu\times V$$\Leftrightarrow$$m = 2,7\times 10^{3}\times 27\times 10^{-3}$
$$\color{Navy}{m = 72,9\,g}$$
- Determine o peso específico no SI para o chumbo, cuja massa específica é $\color{Sepia}{11,34.10^3\,kg/m^3}$. Considere a aceleração da gravidade igual a $ \color{Sepia}{10 m/s^2}$.
$$\color{Maroon}{\rho = \mu\times g}$$
$\rho = 11,34\times 10^{3}\times 10$$\Leftrightarrow$$\rho = 11,34\times 10^{4}$
$$\color{Navy}{\rho = 11,34\times 10^{4}\,N/m^{3}}$$
- Que volume tem um trilho de ferro de massa igual a $\color{Sepia}{3365,4\,kg}$? A densidade do ferro em relação à água é $\color{Sepia}{7,9}$.
$$\color{Maroon}{\delta = \frac{\mu_{Fe}}{\mu_{H_{2}O}}$$
$\mu_{Fe} = \delta_{Fe}\times \mu_{H_{2}O}$$\Leftrightarrow$$\mu_{Fe}= 7,9\times 10^{3}\,kg/m^{3}$
$$\color{Brown}{\mu = \frac{m}{V}}$$
$V = \frac{m}{\mu}$$\Leftrightarrow$$V = \frac{3365,4}{7,9\times 10^{3}}$
$$\color{Navy}{V = 0,426\,m^{3}}$$
Hora de trabalhar um pouco sozinho, não acha!
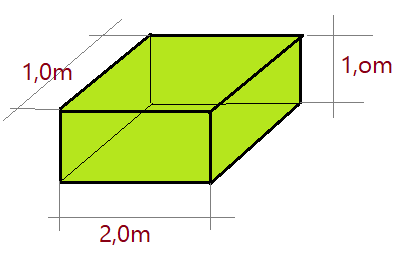
01. Supondo que a figura representa um bloco homogêneo de ferro. Determine a massa específica, sabendo que sua massa é igual a $\color{Sepia}{m = 15.200,0\,kg}$.
02. A massa específica da gasolina é $\color{Sepia}{\mu=0,66\,g/cm^{3}}$. Em um tanque com capacidade para $\color{Sepia}{V= 10000\,l$, qual é a massa de gasolina correspondente?
03. Calcular o peso específico de um cano metálico de $\color{Sepia}{m= 6,0\,kg}$ e cujo volume tubular é de $\color{Sepia}{V = 4\times 10^{-4}\m^{3}}$.
04. O heptano e o octano são duas substâncias que entram na composição da gasolina. Suas massas específicas valem, respectivamente $\color{Sepia}{\mu_{H}= 0,68\,g/cm^{3}}$ e $\color{Sepia}{\mu_{Oc}=0,70\,g/cm^{3}}$. Desejamos saber a densidade da gasolina obtida, misturando-se heptano na proporção $\color{Sepia}{V=65\,cm^{3}}$ e octano $\color{Sepia}{V = 35\,cm^{3}}$.
05. Suponhamos que você possua $\color{Sepia}{m=60\,g}$ de massa de uma substância cujo volume é de $\color{Sepia}{V=5\,cm^{3}}$. Calcule a densidade absoluta (massa específica) dessa substância nas unidades $\color{Sepia}{g/cm^{3}}$e $\color{Sepia}{kg/m^{3}}$ e marque a opção correta.
( )a) $12\,g/cm^{3} e 12\times 10^{-4}\,kg/m^{3}$;
( )b) $1,2\,g/cm^{3} e 12\times 10^{4}\,kg/m^{3}$;
( )c) $14\,g/cm^{3} e 12\times 10^{4}\,kg/m^{3}$;
( )d) $12\,g/cm^{3} e 12\times 10\,kg/m^{3}$;
( )e) $8\,g/cm^{3} e 12\times 10^{-4}\,kg/m^{3}$.
06. Hidrostática é o ramo da Física que estuda as propriedades relacionadas aos líquidos ou gases sob a ação da gravidade em equilíbrio estático. De acordo com o estudo da hidrostática, marque a alternativa que melhor define massa específica.
( )a) massa específica de uma substância é o quociente entre o volume ocupado por uma substância e a massa de uma porção oca de uma substância;
( )b) massa específica é a razão entre a densidade absoluta de uma substância pela densidade de outra substância tomada como padrão;
( )c) massa específica, também chamada de densidade absoluta, de uma substância é a razão entre a massa de uma porção compacta e homogênea dessa substância e o volume ocupado por ela;
( )d) massa específica é a quantidade de matéria que cabe em um volume de um litro dessa substância;
( )e) massa específica é a própria densidade relativa da substância.
07. Calcule a densidade da mistura de dois líquidos homogêneos de massas iguais e massas específicas respectivas de $\color{Sepia}{\mu_{1}=4,2 g/cm^{3}}$ e $\color{Sepia}{\mu_{2}=1,4\,g/cm^{3}}$. Marque a opção correta cuja unidade seja dada em $\color{Sepia}{g/cm^{3}}$.
( )a) $\mu = 2,1\,g/cm^{3}}$;
( )b) $\mu = 5,2\,g/cm^{3}}$;
( )c) $\mu = 1,6\,g/cm^{3}}$;
( )d) $\mu = 0,4\,g/cm^{3}}$;
( )e) $\mu = 2,5\,g/cm^{3}}$.
08. Determine a massa, em $\color{Sepia}{kg}$, de um bloco de ferro maciço em forma de cubo cuja aresta mede $\color{Sepia}{a =10\,cm}$. Suponha que a massa específica do ferro seja igual a $|color{Sepia}{\mu_{Fe}=7,8\,g/cm^{3}}$.
( )a) $m = 78\,kg$;
( )b) $m = 0,78\,kg$;
( )c) $m = 0,0078\,kg$
( )d) $m = 8,7\,kg$
( )e) $m = 7,8\,kg$.
Em caso de dúvidas, faça contato por um dos canais abaixo para esclarecimentos.
Curitiba, 07 de maio de 2015 (Revisado e atualizado em 05/08/2016). Republicação em 25/10/2017).
Décio Adams
www.facebook.com/livros.decioadams
www.facebook.com/decioadams.matfisonline
Telefone: (41) 3019-4760
Celular e WhatsApp: (41) 99805-0732
